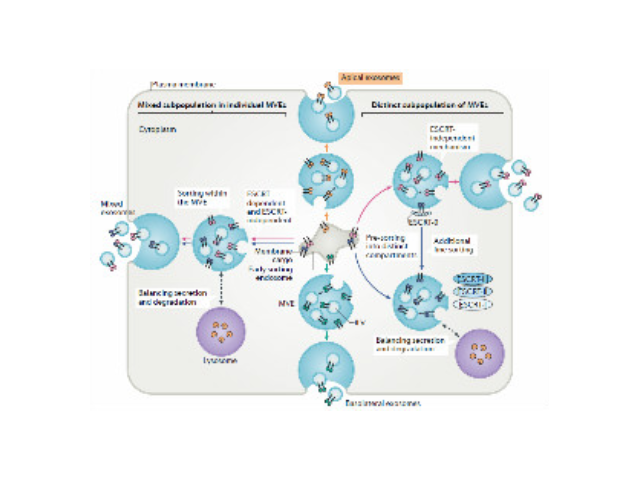
外泌体(Exosome)是细胞主动分泌的囊泡样小体,大小均一,直径30-200nm,密度1.10-1.18g/ml,来源普遍,几乎所有细胞都可分泌,在血液,尿液,唾液,脑脊液,腹水,乳汁等体液中普遍分布。外泌体较早在1986年发现于培养的绵羊红细胞上清液中。1996年,研究者发现外泌体作为抗原呈递因子参与T细胞依赖的抗一些病症反应,开启了外泌体蛋白研究的新天地。2013年诺贝尔生物/医学奖解答了细胞如何组织其内部较重要的运输系统之一——囊泡传输系统的奥秘。一方面可以作为诊断多种疾病的生物指标。开封外泌体提取试剂供应商

外泌体与神经退行性疾病:外泌体可能促进或限制大脑中未折叠和异常折叠的蛋白质的聚集。AD病人脑脊液外泌体中均可检测到Tau和Aβ蛋白。类似的现象也在PD和ALS疾病中发现。PD病人脑脊液外泌体可检测到α-synuclein,ALS病人外泌体中也可以检测到SOD1或TDP-43。外泌体与疾病诊断(应用潜能):外泌体生成机制表明,通过分析外泌体的组分,可以帮助识别其来源的细胞类型。这一特性已被应用于开发心血管疾病,神经系统疾病和一些病症的分子诊断方法,也在肝肾肺相关疾病中进行研发测试。将沉淀物用PBS缓冲液进行悬浮,使外泌体悬浮于液体上层重庆外泌体提取试剂销售厂家磁珠法具有特异性高、操作简便、不影响外泌体形态完整等优点。
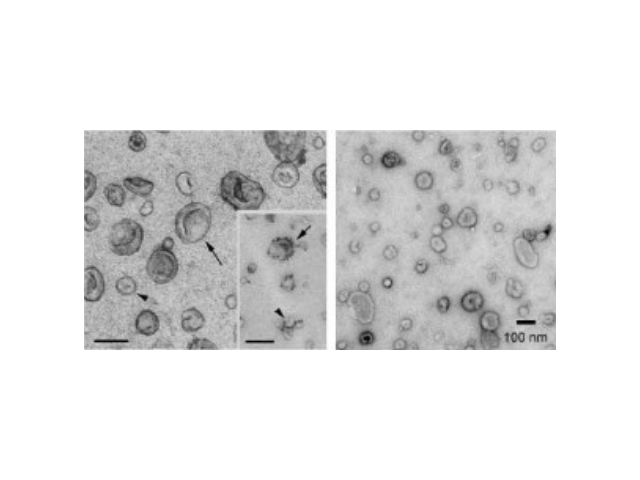
外泌体的提取方法:1、磁珠免疫法。外泌体表面有其特异性标记物(如CD63、CD9蛋白),用包被抗标记物抗体的磁珠与外泌体囊泡孵育后结合,即可将外泌体吸附并分离出来。磁珠法具有特异性高、操作简便、不影响外泌体形态完整等优点,但是效率低,外泌体生物活性易受pH和盐浓度影响,不利于下游实验,难以普遍普及。2、多聚物沉淀法。聚乙二醇(PEG)为常用的多聚物,可与疏水性蛋白和脂质分子结合共沉淀,早先应用于从血清等样本中收集病毒,现在也被用来沉淀外泌体,其原理可能与竞争性结合游离水分子有关。利用PEG沉淀外泌体存在不少问题:比如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物,机械力或者吐温-20等化学添加物将会破坏外泌体等。
外泌体的提取、分离方法:微流控技术。微流控是利用微纳米级尺寸的管道来处理和操控流体所涉及的一门技术,其在外泌体分离方面的应用受到越来越多学者的关注。Jie等[16]课题组开发了一种三维纳米结构微流控芯片,微柱阵列通过化学沉积将交叉多壁碳纳米管功能化,然后其就可以识别特定的分子(CD63)并利用独特拓扑纳米材料高效的捕获外泌体。Wunsch等[17]利用硅工艺生产纳米级确定性侧向位移(Nano-DLD)芯片,得到了均匀的间隙尺寸,该芯片可以灵敏地将20~110nm的颗粒分离。该研究证明了外泌体基于大小的位移,从而揭示了利用芯片分选和量化纳米级生物胶体的潜力。超离法是较常用的外泌体纯化手段,采用低速离心、高速离心交替进行,可分离到大小相近的囊泡颗粒。

这一特性已被应用于开发心血管疾病,神经系统疾病和一些病症的分子诊断方法,也在肝肾肺相关疾病中进行研发测试。将沉淀物用PBS缓冲液进行悬浮,使外泌体悬浮于液体上层,外泌体与神经退行性疾病:外泌体可能促进或限制大脑中未折叠和异常折叠的蛋白质的聚集。AD病人脑脊液外泌体中均可检测到Tau和Aβ蛋白。类似的现象也在PD和ALS疾病中发现。PD病人脑脊液外泌体可检测到α-synuclein,ALS病人外泌体中也可以检测到SOD1或TDP-43。外泌体与疾病诊断(应用潜能):外泌体生成机制表明,通过分析外泌体的组分,可以帮助识别其来源的细胞类型。无法实现临床的常规化应用。重庆外泌体提取试剂销售厂家
外泌体提纯试剂盒的特色与优势:无需沉淀试剂,也无需过夜培养。开封外泌体提取试剂供应商
外泌体的提取方法:1.超速离心法(差速离心)。超离法是较常用的外泌体纯化手段,采用低速离心、高速离心交替进行,可分离到大小相近的囊泡颗粒。超离法因操作简单,获得的囊泡数量较多而广受欢迎,但过程比较费时,且回收率不稳定(可能与转子类型有关),纯度也受到质疑;此外,重复离心操作还有可能对囊泡造成损害,从而降低其质量。2.密度梯度离心。在超速离心力作用下,使蔗糖溶液形成从低到高连续分布的密度阶层,是一种区带分离法。通过密度梯度离心,样品中的外泌体将在1.13-1.19g/ml的密度范围富集。此法获得的外泌体纯度较高,但步骤繁琐,耗时,对离心时间极为敏感。开封外泌体提取试剂供应商
文章来源地址: http://huagong.chanpin818.com/hxsj/shsj/deta_26508736.html
免责声明: 本页面所展现的信息及其他相关推荐信息,均来源于其对应的用户,本网对此不承担任何保证责任。如涉及作品内容、 版权和其他问题,请及时与本网联系,我们将核实后进行删除,本网站对此声明具有最终解释权。



 [VIP第1年] 指数:3
[VIP第1年] 指数:3